Kontakt
Postanschrift
Besuchsanschrift
Elektrochemie und Katalyse an Flüssig-flüssig-Grenzflächen
von Shokoufeh Rastgar
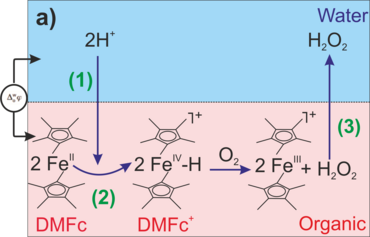
Flüssig/Flüssig-Grenzflächen (L/L liquid-liquid), die zwischen zwei nicht mischbaren Elektrolytlösungen (ITIES, interface between two immiscible electrolyte solutions) gebildet werden, ermöglichen nicht nur die Trennung von Verbindungen durch ihre unterschiedliche Löslichkeit, sondern auch die gleichzeitige Kontrolle und Überwachung der Transferprozesse von Ionen, Elektronen und neutralen Spezies über solche Grenzflächen. Solche Systeme können daher als biomimetische, aber vereinfachte Plattform zur Untersuchung wichtiger Reaktionen in kompartimentierten Reaktionsmedien betrachtet werden.1 Dazu gehören die Reaktion von Ausgangsstoffen in miteinander nicht mischbaren Lösungsmitteln an der Grenzfläche, um organische Substrate zu synthetisieren, und für die Energiewandlung wichtige protonengekoppelte Elektronentransferreaktionen wie die Sauerstoffreduktionsreaktion (ORR) zur Erzeugung von Wasserstoffperoxid (Abbildung 1a)2 und Wasserspaltungsreaktionen3 , wobei der Schwerpunkt entweder auf der Erzeugung von Disauerstoff (O2) 4 oder Wasserstoff (H2) liegt.5,6
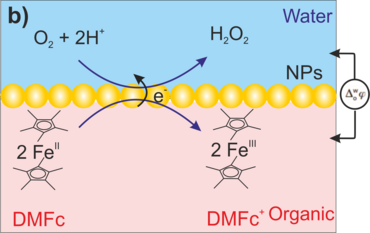
Abbildung 1: Reaktionsschemata der Sauerstoffreduktionsreaktion an einer L/L-Grenzfläche in Gegenwart eines organischen Elektrondonors, Decamethylferrocen; (a) potentialgetriebener H+-Transfer (1), gefolgt von einer homogenen Reaktion zur Erzeugung von H2O2 (2) und dessen Extraktion in die wässrige Phase (3); (b) Grenzflächenreaktion von H+ und O2 zur Erzeugung von H2O2 mit einem Nanokatalysator.
Die L/L-Grenzflächen sind weich, defektfrei und selbstheilend. Die Katalysatoreinheiten, d. h. Metall- oder Metalloxid-Nanostrukturen, können an solchen Grenzflächen angelagert werden (z.B. Abbildung 1b) und als bipolare Elektroden dienen, um die Katalyse durch direkten Elektronentransfer an der Grenzfläche zwischen einer organisch-löslichen Elektronendonor-Spezies, z. B. Metallocenen und molekularem O2, zu erleichtern, wobei der Potenzialabfall an der weichen "Elektroden"-Oberfläche entweder elektrochemisch oder chemisch einstellbar ist. Von besonderem Interesse ist, dass der Nanokatalysator an der L/L-Grenzfläche leicht ausgetauscht werden kann. Im Gegensatz dazu kann keine feste Elektrode diesen Grad an Flexibilität bieten, und die Deaktivierung solcher Einheiten ist nach wie vor ein großes Problem bei fast allen elektrochemischen Reaktionen von Sauerstoff.
Unser Beitrag auf diesem Gebiet
Obwohl Katalysatoren in großem Umfang bei L/L-Prozessen eingesetzt werden, sind detaillierte Studien zur katalytischen Reaktivität und der Produktselektivität über Jahrzehnte hinweg begrenzt geblieben.7,8 Dies ist auf die technische Unzugänglichkeit der kombinierten Transferprozesse von Ionen, Elektronen und neutralen Produkten zurückzuführen, die die photokatalytischen Reaktionen an der L/L-Grenzfläche begleiten. Wir haben verschiedene Konfigurationen der elektrochemischen Rastermikroskopie (SECM, scanning electrochemical microscopy) mit integrierten L/L-Grenzflächen entwickelt, um diese verschränkten Prozesse unabhängig voneinander zu untersuchen.
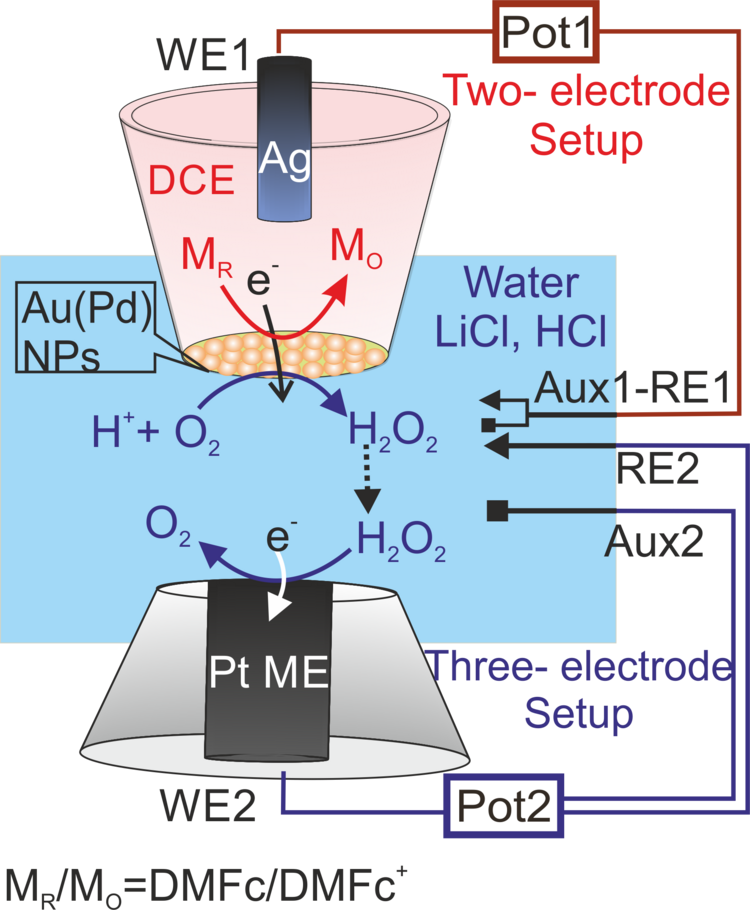
Um die genannten Ziele zu verfolgen, wurden die SECM-Experimente im SG/TC-Modus (substrate-generation/tip-collection) konzipiert.9,10 Ein Schlüsselaspekt ist die mechanische Stabilisierung der L/L-Grenzfläche an der Öffnung einer Mikropipette, was ihre Positionierung in sehr geringem und definiertem Abstand zu einer Mikroelektrode für den Produktnachweis erleichtert. Es wurde für die Sauerstoffreduktionsreaktion an L/L-Grenzflächensystemen mit den Alkalimetallkationen als Phasentransferkatalysatoren angewandt, wobei gezeigt werden konnte, dass ausschließlich der H+-Transfer eine Schlüsselrolle bei der Entstehung von Wasserstoffperoxid an der Grenzfläche spielt (Abbildung 1a).9 In diesem Zusammenhang läuft derzeit das Projekt zur Bestimmung der Reaktivität der Sauerstoffreduktionsreaktion an metallischen (oder bimetallischen) Gold- oder Palladium-Nanopartikeln, die an der L/L-Grenzfläche montiert sind, gleichzeitig mit dem Nachweis von H2O2 (Abbildung 2).
Darüber hinaus haben wir die Anwendung des vorgeschlagenen Ansatzes erweitert, indem wir Lichtpulse an eine solche Konfiguration koppelten, um die photochemischen katalytischen Reaktionen an der mit BiVO4 -Nanopartikeln modifizierten L/L-Grenzfläche10-12 lokal zu verfolgen und gleichzeitig die Produkte der Wasseroxidationsreaktion nachzuweisen, entweder O2 (als Hauptprodukt, Abbildung 3a, 3b)11 oder die reaktiven Sauerstoffspezies (z.B., adsorbiertes OH· ) (Abbildung 3c, 3d).10 Im letzteren Fall haben wir den Oberflächentitrationsmodus (SI, surface interrogation) der SECM an einer L/L-Grenzfläche verwendet, um die photogenerierten Oberflächenzwischenprodukte während der Wasseroxidation an BiVO4-Nanopartikeln zu nachzuweisen.10 (Abbildung 3c). Die SECMx-Software wurde in unserer Gruppe erweitert, um vordefinierte Potential- und Lichtpulse anzulegen, die Verbindung zur Elektrode zu schalten und Stromtransienten während der Licht- und Potentialpulse aufzuzeichnen (Abbildung 3d). In diesen Fällen wurde der Potentialabfall an der L/L-Grenzfläche chemisch eingestellt.
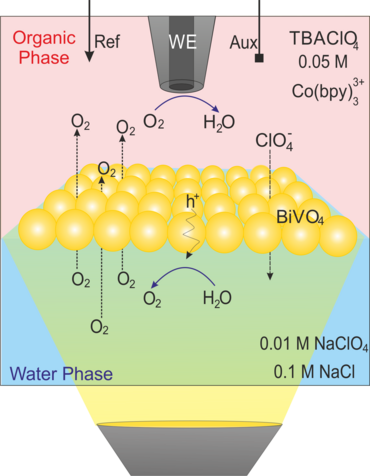
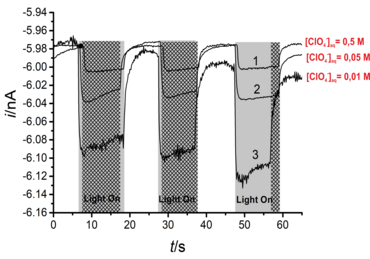
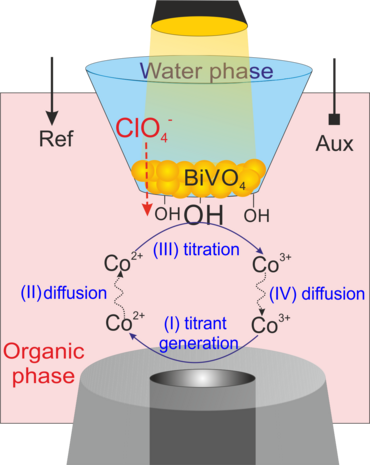
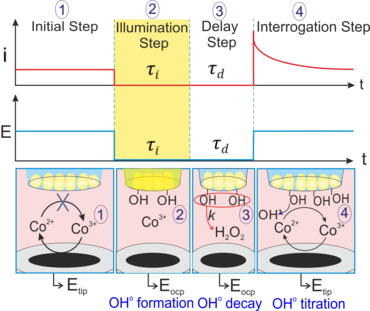
Abbildung 3: (a) Schematische c Darstellung des SECM SG/TC-Modus für die lokale Detektion von photokatalytisch erzeugtem O2 ; (b) Transiente Ströme für die Reduktion von photoerzeugtem O2 durch ClO4− Ionentransfer bei unterschiedlichen Konzentrationen von ClO4− in wässriger Phase. Weitere Einzelheiten in unserer veröffentlichten Arbeit;11 (c) schematische c Darstellung des SI-SECM-Aufbaus zur quantitativen Bewertung der Oberflächen-Zwischenprodukte OH•ads der photochemischen Reaktion und ihres Zerfallsprozesses. Als Titriermittel wurde [Co(bpy) ]33+ verwendet; (d) Versuchsablauf für das Anlegen der Potential- und Lichtpulse und die Aufzeichnung der Stromtransienten für die Erzeugung und den Nachweis von OH•ads auf der BiVO4 Oberfläche.
Literatur
- K. Piradashvili, E. M. Alexandrino, F. R. Wurm und K. Landfester, Reactions and Polymerizations at the Liquid-Liquid Interface, Chem. Rev., 2016, 116, 2141-2169.
- B. Su, R. P. Nia, F. Li, M. Hojeij, M. Prudent, C. Corminboeuf, Z. Samec und H. H. Girault, H O22 Generation by Decamethylferrocene at a Liquid|Liquid Interface, Angew. Chem. Int. Ed., 2008, 47, 4675-4678.
- M. D. Scanlon, P. Peljo, L. Rivier, H. Vrubel und H. H. Girault, Mediated Water Electrolysis in Biphasic Systems, Phys. Chem. Chem. Phys., 2017, 19, 22700-22710.
- S. N. M. Betancourt, J. S. Riva, J. G. Uranga, A. J. Olaya und H. H. Girault, Visible-light Driven Water Oxidation and Oxygen Production at Soft Interfaces Chem. Commun. 2022, 58, 3965-3968.
- L. Rivier, P. Peljo, L. A. C. Vannay, G. C. Gschwend, M. A. Méndez, C. Corminboeuf, M. D. Scanlon und H. H. Girault, Photoproduction of Hydrogen by Decamethylruthenocene Combined with Electrochemical Recycling, Angew. Chem. Int. Ed., 2017, 56, 2324-2327.
- P. Ge, M. Hojeij, M. D. Scanlon und H.H. Girault, Photo-recycling the Sacrificial Electron Donor: Towards Sustainable Hydrogen Evolution in a Biphasic System, ChemPhysChem, 2020, 21, 2630-2633.
- A. G. Quijano, G. Herzog, P. Peljo, M.D. Scanlon, Electrocatalysis at the Polarised Interface Between Two Immiscible Electrolyte Solutions, Curr. Opin. Electrochem., 2023, 38,101212, DOI:10.1016/j.coelec.2023.101212.
- M. Opallo, K. Dusilo, M. Warczak, J.Kalisz, Hydrogen Evolution, Oxygen Evolution, and Oxygen Reduction at Polarizable Liquid|Liquid Interfaces, ChemElectroChem, 2022, 9, e202200513.
Eigene Beiträge zum Forschungsgebiet
- S. Rastgar, K. Teixeira Santos, C. A. Angelucci, G. Wittstock
Catalytic activity of alkali metal cations for chemical oxygen reduction reaction in a biphasic liquid system probed by scanning electrochemical microscopy
Chem. Eur. J. 2020, 26, 10882-10890. Abstract & Link (Open Access)
- S. Rastgar, G. Wittstock
In Situ Microtitration of Intermediates of Water Oxidation Reaction at Nanoparticles Assembled at Water/Oil Interfaces
J. Phys. Chem. C, 2018, 122, 12963−12969. Abstract & Link
- S. Rastgar, G. Wittstock
Characterization of Photoactivity of Nanostructured BiVO4 at Polarized Liquid-Liquid Interfaces by Scanning Electrochemical Microscopy
J. Phys. Chem. C 2017, 121, 25961-25948. Abstract & Link
- S. Rastgar, M. Pilarski, G. Wittstock
Polarized liquid-liquid interface meets visible light-driven catalytic water oxidation
Chem. Commun. 2016, 52, 11382-11385. Abstract & Link - W. Adamiak, J. Jedraszko, W. Nogala, M. Jönsson-Niedziolka, S. Dongmo, G. Wittstock, H.H. Girault, M.Opallo
A Simple Liquid–Liquid Biphasic System for Hydrogen Peroxide Generation
J. Phys. Chem. C, 2015, 119 (34), 20011–20015, Abstract & Link - J. Jedraszko, W. Nogala, W. Adamiak, S. Dongmo, G. Wittstock, H. H. Girault, M. Opallo
Catalysis at room temperature ionic liquid|water interface: H2O2 generation
Chem. Commun. 2015, 51, 6851-6853, Abstract & Link