Kontakt
Postanschrift
Besuchsanschrift
Modellsysteme für die Magnetrezeption an Oberflächen: Flavine und Cryptochrom 4a
von Moritz Bätcher

Überblick
Im Rahmen des Exzellenzclusters NaviSense (Link) untersuchen wir die Bindung des flavinhaltigen Redoxproteins Cryptochrom 4a an Oberflächen. Dieses Protein wird in Verbindung zur Magnetrezeption von Zugvögeln gebracht wird.[1] Redoxproteine sind Proteine, die an Oxidations- und Reduktionsprozessen beteiligt sind. Unser Fokus liegt auf der Synthese von modifizierten Oberflächen, die das Redoxprotein spezifisch, ausgerichtet und unter Erhalt der Proteinstruktur binden, um die gebundenen Proteine danach mit Kooperationspartner spektroskopisch untersuchen zu können. Zur gerichteten Bindung werden funktionalisierte selbstassemblierte Monolagen (Link) genutzt.
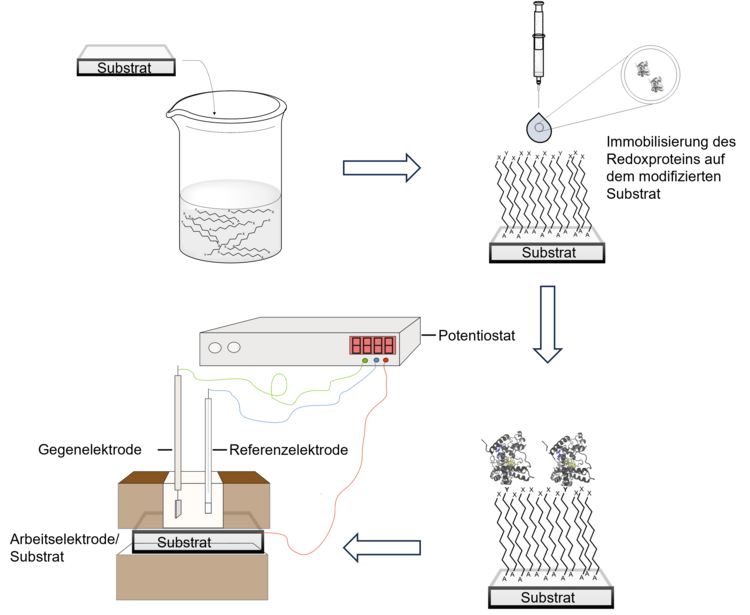
Methoden zur Charakterisierung modifizierter Oberflächen
Flavinhaltige Modellverbindungen zur Untersuchung von Elektronentransfereigenschaften
Mit Modellverbindungen versuchen wir künstliche Systeme nachzubauen, die ein ähnliche Reaktion auf schwache Magnetfelder zeigen wie Cryptochrome 4a. Dadurch wollen wir verstehen, welche strukturellen Eigenschaften für diese molekularen Sensoren notwendig sind.
Die zentrale funktionelle Gruppe in Chryptochrom 4a ist Flavin-adenin-dinucleotid (FAD+). Flavin ist eine der redoxaktive Gruppen im Protein Cryptochrom 4a und geht je nach lokaler Umgebung sehr unterschiedliche Redoxreaktionen ein, die sich in Modellsystemen untersuchen lassen. Solche Reaktionen werden als protonengekoppelte Elektronentransferreaktionen (PCET-Reaktionen – proton-coupled electron transfer reactions) bezeichnet.

Die gezielte Bindung dieser Modellverbindungen an Elektrodenoberflächen ermöglicht es, den Elektronentransfer zwischen Flavinen und einer Elektrode systematisch zu untersuchen. Die so gewonnenen Ergebnisse dienen als Referenzdaten, um den vorgeschlagenen Mechanismus der Magnetrezeption besser verstehen zu können. Die Verwendung von gemischten Monolagen ermöglicht die Einstellung der molekularen Umgebung des Flavins und stellt somit eine Möglichkeit dar, die Umgebung der Flavingruppe innerhalb des Redoxproteins Cryptochrom 4a zu imitieren. Solche gemischten Monolagen entstehen durch die Kombination verschiedener Adsorbatmoleküle, von denen ein Teil funktionelle Endgruppen zur Proteinbindung trägt, während andere Moleküle keine Bindungsendgruppen tragen und somit die Funktionalität verdünnen (diluents).
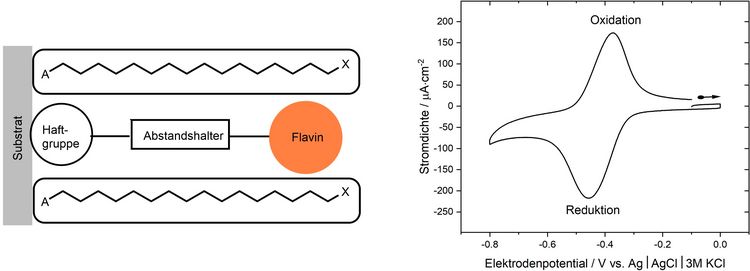
Cyclovoltammetrische Messungen zeigen, dass Flavine in wässrigen Pufferlösungen ein besonderes Redoxverhalten besitzen. Das oxidierte Flavin wird dabei in einem Schritt durch die Aufnahme von zwei Elektronen und zwei Protonen zum Flavohydrochinon reduziert. Ein radikalisches Zwischenprodukt kann unter diesen Bedingungen nicht beobachtet werden, da das zweite Elektron bei einem positiveren Potential übertragen wird als das erste. Im Gegensatz dazu lassen sich in hydrophober Umgebung auch Ein-Elektronentransferreaktionen mittels voltammetrischen Methoden charakterisieren.[2]
Weiterführende Literatur
[1] P. J. Hore, H. Mouritsen; The Radical-Pair Mechanism of Magnetoreception. Annu. Rev. Biophys. 2016, 45, 299-344. https://doi.org/10.1146/annurev-biophys-032116-094545
[2] S. L. J. Tan, R. D. Webster; Electrochemically Induced Chemically Reversible Proton-Coupled Electron Transfer Reactions of Riboflavin (Vitamin B2). J. Am. Chem. Soc. 2012, 134, 5954-5964. https://doi.org/10.1021/ja300191u

