Entwicklung eines dreidimensionalen Tränendrüsengewebes in vitro
Kontakt
Direktor der Universitätsklinik für Augenheilkunde
Leitung des Labors für Experimentelle Ophthalmologie
Sekretariat im Pius-Hospital Oldenburg
Anschrift
Lehrbeauftragte:
Entwicklung eines dreidimensionalen Tränendrüsengewebes in vitro
Die Tränendrüseninsuffizienz ist eine der Hauptursachen für die Entwicklung des Krankheitsbildes des Trockenen Auges (Keratokonjunktivitis sicca, engl.: Dry Eye Syndrome, DES), welches zu Schmerzen, Beeinträchtigungen der Sehkraft und des Kontrastsehens und in schwersten Fällen zu einem vollständigen Verlust der Sehkraft führen kann.
Eine der Hauptursachen der DES ist die Funktionsstörung der Tränendrüse (TD). Diese kann altersbedingt sein, jedoch auch durch chronisch verlaufende Autoimmunerkrankungen wie das Sjögren-Syndrom ausgelöst werden. Das Sjögren-Syndrom manifestiert sich in einer morphologischen Veränderung der Tränen- und Speicheldrüse, welche durch entzündliche Prozesse angegeriffen werden. In diesem Fall wird Tränenflüssigkeit entweder gar nicht oder nur sehr vermindert produziert oder die Zusammensetzung der wässrigen Phase des Tränenfilms ist stark verändert. Die weltweite Prävalenz eines Dry Eye Syndrome wird je nach Altersklasse (21 - >65Jahren) auf fünf bis 35 Prozent geschätzt. Bis heute gibt es keine erfolgreichen kurativen Therapieoptionen, sodass Patienten neben dem intensiven Gebrauch von Tränenersatzmitteln, die Nutzung speziell angefertigten Flüssigkeitskammer-Brillen oder ein Verschluss der Tränenpünktchen durch sogenannte „punctum plugs“ oder durch Verödung bleibt. Diese Maßnahmen führen bei schweren Fällen des trockenen Auges jedoch nur selten zu einer anhaltenden Beschwerdefreiheit.
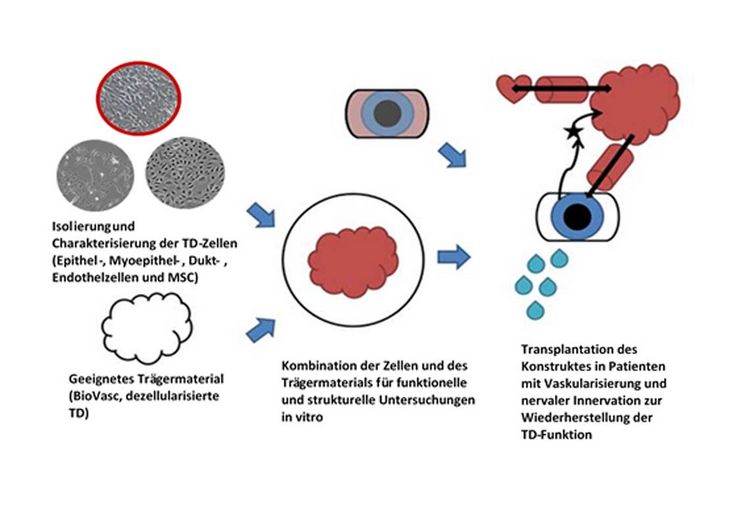
Ein neuer und vielversprechender Therapie-Ansatz stellt die Rekonstruktion einer dreidimensionalen, funktionell aktiven Tränendrüse (TD) mittels sogenannter „Tissue Engineering“ Methoden dar, was die Grundlage dieses Projektes ist.
Die Basis dieses Konstruktes ist ein zellfreies Gewebe (sogenannter BioVasc (Teilstücke des Darms) und Tränendrüse) vom Hausschwein (sus scrofa). Neben der guten Verfügbarkeit und der bereits klinisch bewiesenen Biokompatibilität von porcinem Gewebe (als Beispiel sind hier die bereits jahrelang genutzten Herzklappen-Ersatzgewebe von Schweinen zu nennen), bietet diese zellfreie Matrix die strukturell notwendigen Gegebenheiten, wie zum Beispiel das Vorhandensein von Gefäß- und Oberflächenstruktur, welche für eine erfolgreiche Rekonstruktion einer TD notwendig sind. Für die Rekonstruktion einer funktionell aktiven TD ist neben der geeigneten Trägermatrix die genaue Zusammensetzung der Zellpopulation von entscheidender Bedeutung. In einer Tränendrüse finden sich neben den gefäßauskleidenden Endothelzellen, die funktionell aktiven Azinus- und Duktuszellen (Epithelzellen) und die mesenchymalen Stammzellen.
Im Rahmen des Projektes wurden daher bereits die unterschiedlichen Zelltypen aus porcinen Tränendrüsen isoliert, kultiviert und auf ihre sekretorische Aktivität in der Zellkultur untersucht. Nachfolgend konnte durch Nutzung aller drei Zelltypen organoid-ähnliche Strukturen (sogenannte Spheroide) generiert werden und auf dezellularisiertes porcines Trägermaterial aufgebracht werden. Unter dynamischen Kulturbedingungen in einem Bioreaktor sezernierten die Spheroide aktiv verschiedene in der Tränenflüssigkeit vorkommende Substanzen. Nach diesen erfolgreichen ersten Versuchen soll in diesem Projekt die Komplexität der 3D-Struktur durch Nutzung eines BioVasc®-Systems (und dem damit vorhandenen Gefäßsystems) der Struktur einer Tränendrüse angepasst werden.
Hauptziel der Studie stellt die Untersuchung dar, in welchem Umfang eine Vaskularisierung des dreidimensionalen Trägermaterials das Einwachsen und die Funktionalität der eingebrachten Tränendrüsenzellen beeinflusst. Die Analyse der verschiedenen Systeme erfolgt mittels immunhistologischer und funktioneller Untersuchungen. Es wird sowohl die Morphologie der Konstrukte, als auch die Sekretionskapazität geprüft. Diese Ansätze bilden die Grundlage für geplante in vivo Versuche, bei denen funktionell aktive und vaskularisierte Konstrukte in Tiere transplantiert werden, um eine geschädigte Tränendrüse zu ersetzen. Dies stellt eine mögliche neue Therapieoption des Dry Eye Syndroms dar.