Forschung
Kontakt
Sekretariat Forschung
Anschrift
Forschung
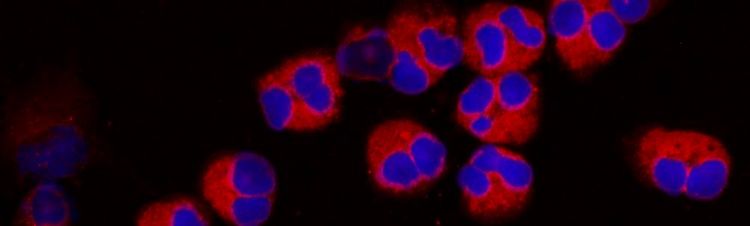
Forschung der Abteilung für Experimentelle Allergologie und Immundermatologie
Der Schwerpunkt unserer Forschungsgruppe liegt auf Autoimmunerkrankungen wie dem bullösen Pemphigoid, Allergien, Hautkrebs und entzündlichen Hauterkrankungen einschließlich atopischer Dermatitis, Kontaktekzemen und Psoriasis. Wir sind besonders an der Rolle von Basophilen und Eosinophilen bei diesen Erkrankungen interessiert, da die aus diesen Zellen freigesetzten Entzündungsmediatoren eine entscheidende Rolle in der Schwere der Symptome spielen und auch auf andere Immunzellen einwirken, die diese Krankheiten steuern. Unsere Gruppe verfügt über langjährige Erfahrung in der Isolierung und Reinigung von menschlichen allergischen Effektorzellen, um deren funktionelle Reaktionen zu untersuchen und um die intrazellulären Signalmechanismen aufzuklären, die ihre Reaktivität kontrollieren. Unser Hauptziel ist es, die verschiedenen Rollen dieser Zellen bei Autoimmunität und Allergien zu verstehen und neue therapeutische Strategien zu entwickeln.
Zu den laufenden internationalen Forschungskooperationen zählen die Universität Groningen (NL), wo wir die Ursachen für die Blasenbildung der Haut beim bullösen Pemphigoid und die Rolle von TRP Kanälen bei atopischer Dermatitis untersuchen.
Zudem sind wir Mitglied der translationalen PruSeach Forschergruppe, die von der Deutschen Forschungsgemeinschaft (DFG) gefördert wird. In enger Kooperation mit der Universität Heidelberg, Düsseldorf, Münster, Mainz, Erlangen und Würzburg hoffen wir die neuartigen Mechanismen des Juckreizes und seiner Verbindung zum Schmerz zu enträtseln und neue Behandlungsziele zu identifizieren. Weitere Kooperationspartner sind die Unversität Leuven (Belgien) und die Medizinische Hochschule Hannover, mit denen wir an grundlegenden Fragestellungen zur Rolle von Entzündungsmediatoren bei chronisch entzündlichen Hauterkrankungen forschen.
Bullöses Pemphigoid
Das bullöse Pemphigoid (BP) ist eine blasenbildende Autoimmundermatose, die in den Formenkreis der seltenen Autoimmunerkrankungen gehört. Die Beschwerdesymptomatik des bullösem Pemphigoides wird anfänglich durch Juckreiz mit Erythemen und später mit dem Aufschießen von prallen Blasen beschrieben. Vornehmlich tritt das bullöse Pemphigoid bei älteren Menschen auf. Die Ätiologie des bullösen Pemphigoides wird durch die Bildung von IgG-Autoantikörpern gegenüber hemidesmosomalen Antigenen wie dem Bullösen Pemphigoid Antigen 1 (BP230) und dem Bullösen Pemphigoid Antigen 2 (BP180) erklärt. BP180 ist ein transmembranöses Mitglied des Kollagen Proteins Typ XVII, das als primäres antigenes Target von BP Autoantikörpern identifiziert wurde. BP180 wird auf der basalen Oberfläche basaler epidermaler Keratinozyten exprimiert und ist ein Glied des hemidesmosomalen Komplexes, einer zellulären Struktur, die als dermo-epidermale Adhaesion fungiert. Die Hauptepitope von BP180, die mit der Krankheit assoziiert sind, werden auf der NC16A Domäne abgebildet. Neben den IgG Auto-AK spielen auch IgE AK eine pathogenetische Rolle beim bullösen Pemhpigoid.
Charakteristisch für das bullöse Pemphigoid ist ein massives Infiltrat eosinophiler Granulozyten. Die Blasenbildung wird nicht nur durch die Bindung der Auto-AK, sondern auch durch das hauptächlich granulozytäre Infiltriat, Komplement und Eosinophilenproteasen bedingt. Zudem ist die Anzahl der basophilen Granulozyten in der Dermis bei Patienten mit bullösem Pemphigoid erhöht.
Wir interessieren uns beim bullösen Pemphigoid insbesondere für die Rolle der basophilen und eosinophilen Granulozyten. Die Forschung wird unter anderem über die DFG gefördert. Zudem besteht eine Forschungskooperation mit der Arbeitsgruppe von Prof Dr. Marcel Jonkman vom UMCG Groningen, in der wir gemeinsam die Ursachen für die Blasenbildung der Haut beim bullösen Pemphigoid im Rahmen eines Joint-Ph.D. Programmes untersuchen (Project 4: “Bullous pemphigoid – What makes the blister?”).
Chronischer Pruritus
Chronischer Pruritus ("chronischer Juckreiz ") ist eines der häufigsten Symptome vieler Hauterkrankungen und kann die Lebensqualität erheblich verschlechtern. Chronische, entzündliche Hauterkrankungen, einschließlich Lichen planus (LP), Psoriasis (PSO) und atopische Dermatitis (AD), sind eine Hauptursache des chronischen Pruritus. Dennoch unterscheiden sich diese Erkrankungen grundlegend in Bezug auf Phänotyp, Histopathologie und immunologische Prinzipien, die dem Krankheitsverlauf zugrunde liegen. Es gibt zunehmend Hinweise darauf, dass IL-17, IL-31, NGF und TSLP eine entscheidende Rolle bei der Pruritusbildung spielen. Es wurde gezeigt, dass therapeutische Antikörper, die entweder auf IL-17A oder IL-31A abzielen, Juckreiz bei PSO bzw. AD wirksam reduzieren.
Die molekulare Grundlage des chronischen Pruritus bei Hautentzündungen ist jedoch noch weitgehend ungeklärt.
Unser Hauptziel ist die Charakterisierung bekannter (IL-31, NGF, TSLP) und die Identifizierung neuer Pruritus Signalwege bei chronischer Hautentzündung mittels Transkriptom- und Zytokinanalysen von hautinfiltrierenden T-Zellen, Mastzellen und eosinophilen Granulozyten sowie von peripheren mononukleären Blutzellen (PBMCs), um neue Therapiemöglichkeiten zu erschließen.
Unsere Arbeitsgruppe ist Teil der Translational Pruritus Forschergruppe (Translational Pruritus Research, PruSearch FOR 2690), die von der Deutschen Forschungsgemeinschaft (DFG) gefördert wird.
Die Forschergruppe besteht aus Wissenschaftlern und Experten auf dem Gebiet der Pruritusforschung in Deutschland mit verschiedenen Fachgebieten wie Dermatologie, Neurophysiologie, Anästhesiologie, Neurologie, Gastroenterologie und Radiologie.
Im Rahmen dieser Forschergruppe identifizieren und charakterisieren wir gemeinsam mit der Arbeitsgruppe von Prof Dr. Bernhard Homey vom UKD Düsseldorf die Pruritus Signalwege bei chronischen Hautentzündungen (Projekt 5: Identifizierung und Charakterisierung von Pruritus Signalwegen bei chronischer Hautentzündung).
TRP-Kanäle
Die Atopische Dermatitis (AD) ist eine chronisch juckende und entzündliche Hauterkrankung, die die Lebensqualität der Patienten stark beeinträchtigt. Der Mechanismus des chronischen Juckreizes bei AD ist bisher noch nicht vollständig geklärt. Eosinophile und basophile Granulozyten sind für die Auslösung und Aufrechterhaltung der Entzündung bei atopischer Dermatitis verantwortlich. In diesem Zusammenhang haben wir gezeigt, dass eine bidirektionale Interaktion zwischen Eosinophilen und peripheren Nerven eine Rolle bei der AD-Pathologie spielt. Es gibt immer mehr Belege dafür, dass TRP-Kanäle (Transient Receptor Potential) an den Mechanismen der Neuro-Immun-Interaktion in Bezug auf Juckreiz und Entzündungen beteiligt sind. TRP-Kanäle werden hauptsächlich von sensorischen Neuronen exprimiert, aber neuere Studien haben gezeigt, dass sie auch in Immunzellen, T-Zellen und Neutrophilen, funktionell exprimiert werden. Durch die Aufrechterhaltung der intrazellulären Kalziumhomöostase regulieren TRP-Kanäle verschiedene Funktionen dieser Zellen, wie z. B. die Freisetzung juckreizauslösender und proinflammatorischer Mediatoren, die Zellmigration und den Zelltod.
Ziel dieses Translationsprojekts ist es, die Expression und Funktion von TRP-Kanälen zu charakterisieren.
Das Projekt wird durch den Forschungspool der Fakultät für Medizin und Gesundheitswesen der Universität Oldenburg (Atopic Dermatitis - novel functions of TRP channels in neuro immune interaction mechanism; uol.de/medizin/forschungspool/uebersicht-gefoerderter-forschungspoolprojekte) finanziert.
„Role of IL-31/IL-31RA axis in human Neutrophils in pruritic
skin inflammation“
Die atopische Dermatitis (AD) ist eine chronische, juckende und entzündliche Hauterkrankung, die die Lebensqualität der Patienten stark beeinträchtigt. Die Mechanismen des chronischen Juckreizes und der Entzündung bei der Neurodermitis sind noch nicht vollständig geklärt. Im Allgemeinen wird Juckreiz durch ein komplexes Zusammenspiel von Entzündungsmediatoren, Immunzellen, Hautzellen und neuronalen Netzwerken vermittelt. Neutrophile Granulozyten sind für die Auslösung und Aufrechterhaltung der Entzündung bei AD verantwortlich. Ein Schlüsselmediator und Bindeglied zwischen Immunzellen und Neuronen bei Pruritus ist das Zytokin Interleukin-31 (IL-31), dass die Neuronenaussprossung fördert. IL-31 wird von verschiedenen Immunzellen wie T-Zellen, Eosinophilen und Basophilen sezerniert und über einen Rezeptorkomplex, bestehend aus dem IL-31-Rezeptor alpha (IL-31RA) und dem Oncostatin-M-Rezeptor beta (OSMRβ), signalisiert. In diesem Zusammenhang konnten wir die Expression von IL-31 auf Eosinophilen und Basophilen und die Expression der Rezeptoren IL-31RA und OSMRβ auf Basophilen nachweisen. Ziel dieses Translationsprojekts ist es, die Expression und Modulation von IL-31RA und OSMRβ sowie die funktionelle Rolle von IL-31 auf Neutrophilen zu untersuchen.
Das Projekt wird durch den Forschungspool der Fakultät für Medizin und Gesundheitswesen der Universität Oldenburg („Role of IL-31/IL-31RA axis in human neutrophils in pruritic skin inflammation“) uol.de/medizin/forschungspool/uebersicht-gefoerderter-forschungspoolprojekte) finanziert.
