Entwicklung und Charakterisierung künstlicher Materialien für die Augenoberflächenrekonstruktion
Kontakt
Direktor der Universitätsklinik für Augenheilkunde
Leitung des Labors für Experimentelle Ophthalmologie
Sekretariat im Pius-Hospital Oldenburg
Anschrift
Lehrbeauftragte:
Entwicklung und Charakterisierung künstlicher Materialien für die Augenoberflächenrekonstruktion
Die menschliche Kornea (Augenhornhaut) gehört zum vorderen Augenabschnitt und ist von essentieller Bedeutung für das Sehvermögen. Sie ist etwa 500 µm dick und besteht im Wesentlichen aus drei zellulären Schichten: dem außenliegenden Epithel, dem Stroma und dem innenliegenden Endothel, welche durch zwei dünne azelluläre Schichten, Bowman-Lamelle und Descemet-Membran, voneinander getrennt werden. Das Stroma macht circa 90 Prozent der Hornhautdicke aus und besteht selbst zu 75 Prozent aus Wasser, drei bis zehn Prozent Keratozyten und extrazellulärer Matrix. Diese extrazelluläre Matrix wird von den Keratozyten sezerniert und besteht im Wesentlichen aus Kollagen und Proteoglykanen.
Erkrankungen der Augenoberfläche, wie zum Beispiel die neurotrophe Keratopathie, okuläres Pemphigoid, Stevens-Johnson Syndrom, Infektionen oder Verbrennungen/Verätzungen können zu Hornhauterosionen, Bildung von Hornhautgeschwüren, Substanzdefekten und Narbenbildung führen. Dies kann mit einer Beeinträchtigung der Transparenz und der Oberflächenkrümmung der Kornea einhergehen und so eine Minderung des Sehvermögens, bis zum vollständigen Verlust der Sehfähigkeit führen.
Weltweit sind pathologische Veränderungen der Kornea nach der Katarakt und dem Glaukom die dritthäufigste Ursache für Erblindung. Für die meisten dauerhaften Funktionsstörungen der Kornea gibt es keine medikamentösen Therapieoptionen, sodass häufig nur chirurgische Maßnahmen das Sehvermögen des Patienten erhalten bzw. wiederherstellen können. Zur Abheilung persistierender oder progredienter Hornhautepitheldefekte wird zumeist Amnionmembran (die innerste Membran der Fruchtblase; kurz AM) verwendet. Diese kann als transferable Abdeckung zum mechanischen Schutz des regenerierenden Hornhautepithels (Onlay) oder als Transplantat, das in den Hornhautdefekt eingebracht wird und dort als Basalmembranersatz fungiert (Inlay), eingesetzt werden. AM weist eine vorteilhafte zellwachstumsstimulierende, antientzündlichen und antiangiogenetische Wirkung auf. Als Nachteile sind allerdings die schlechte Standardisierbarkeit des Gewebes, die Gefahr einer Infektionsübertragung von Spender auf Empfänger sowie die deutlich eingeschränkte Transparenz zu nennen, wodurch postoperativ die Sehfunktion eingeschränkt wird. Zudem führt die geringe biomechanische Festigkeit des Gewebes häufig zu einem Verlust des Transplantates.
Für die Therapie stromaler Hornhautdefekte wird eine Transplantation von humanem Spenderhornhautgewebe in Form einer lamellaren oder perforierenden Keratoplastik durchgeführt, um die Sehfähigkeit wiederherzustellen. Als limitierender Faktor steht hierbei neben der Gefahr der Transplantatabstoßung vor allem die begrenzte Verfügbarkeit von geeignetem Spendermaterial im Vordergrund. Aus diesem Grund sind derzeit sowohl Alternativen zur Amnionmembrantransplantation als auch zur Transplantation von humanen Spenderhornhäuten Gegenstand dieser Forschungsprojekte. Dabei werden zwei verschiedene Ansätze verfolgt: zum einen die Nutzung körpereigener Zellen, die zur Synthese einer Matrix angeregt werden und so eine hohe Biokompatibilität für die Patienten aufweisen, und zum anderen Matrices aus Biomaterialien, welche standardisiert und GMP-konform hergestellt werden können.

In-vitro kultivierter humanen kornealen Stroma-Ersatz zur Augenoberflächenrekonstruktion
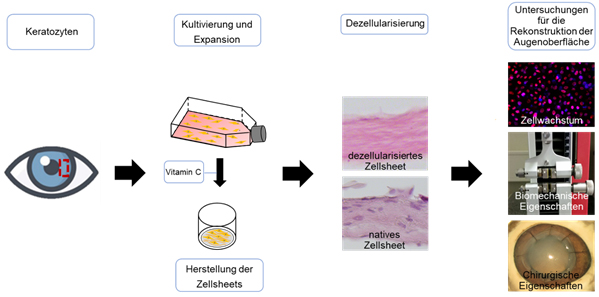
Ein vielversprechender Ansatz für die Rekonstruktion des Hornhautstromas ist die Stimulation von humanen kornealen Keratozyten zur Sekretion von extrazellulärer Matrix. Vorteil eines solchen in-vitro erzeugten Ersatzgewebes ist die Möglichkeit der Herstellung aus dem jeweiligen Zellmaterial des Empfängers, sodass Abstoßungsreaktionen gegen das Spendergewebe sowie das Risiko einer Infektionsübertragung vom Spender auf den Empfänger ausbleibt. Die Stimulation der Synthese extrazellulärer Matrix kann dabei sehr effektiv durch Supplementierung von Keratozyten-Kulturen mit Vitamin C erfolgen. Die Stimulation von humanen Keratozyten zur Sekretion kollagenhaltiger extrazellulärer Matrix induziert durch Vitamin C oder Vitamin C-Derivate führt zu Zellsheets mit hoher Zelldichte. Diese Konstrukte ähneln der Matrix, die in vivo während der kornealen Entwicklung auftritt und werden deshalb als vielversprechende Ansätze für die In-vitro-Generierung stromalen Gewebes betrachtet. In ersten Versuchen konnten wir bereits zeigen, das durch eine 12 monatige Kultivierung der Zellsheets eine Materialdicke von 100µm erzeugt werden kann, was für eine Transplantation als Stromaersatz relevant ist. Weiterhin wurden die stabilen Zellsheets dezellularisiert, was zu einem zellfreien Konstrukt führte, was eine erhöhte Biokompatibilität aufweist. Diese Zellsheets wurden auf ihre Materialeigenschaften, Nähbarkeit und auf ihre Eigenschaften als Wachstumssubstrat für Zellen untersucht.
Nachfolgend werden die Eigenschaften der generierten Zellsheets in einem Tiermodell sowie deren GMP-konforme, standardisierte Herrstellung untersucht, um diese Matrices später in Patienten nutzen zu können.
Substanz-beladene Kollagen-Gele und Keratinfilme
Aufgrund der bisher schlechten Spenderrate für Hornhäute und der Problematik mit möglichen Abstoßungsreaktionen etc., ist der Bedarf an der Entwicklung von neuen Hornhaut- und Bindehautersatzgeweben sehr groß. Diese künstlichen Gewebe müssen unter anderem biokompatibel sein, geringe Qualitätsunterschiede aufweisen, sich als Wachstumssubstrat für Augenoberflächenepithelzellen eignen, biomechanisch über einen langen Zeitraum stabil bleiben und sicher bei der Verwendung beim Menschen sein. Aufgrund dieser Anforderungen ist die Suche nach geeigneten Biomaterialien sehr schwierig, jedoch wurden in den letzten Jahren vielversprechende Ansätze beschrieben. In Zusammenarbeit mit der Arbeitsgruppe von Prof Dr. Reichl (Technische Universität Braunschweig) und Prof Dr. Hansmann (TERM, Würzburg) haben wir bereits Kollagengele (auf Basis von Collagen 1) und Keratinfilme (auf Basis von Haarkeratin) als Materialien für die Augenoberflächenrekonstruktion eingehend in vitro und in vivo untersucht. Unsere früheren Arbeiten haben gezeigt, dass Keratin-basierte Matrizen für die Rekonstruktion der Hornhautoberflächen in vitro und in vivo erfolgreich eingesetzt werden können. Außerdem wurde die erfolgreiche Verwendung von komprimierten Kollagengelen als Matrix für den konjunktivalen Ersatz in vitro und in vivo gezeigt.
Ziel dieses Projekts ist es, diese Konstrukte für den Hornhaut- und Bindehautersatz weiter zu verbessern, um gezielt bestimmte klinische Probleme bei der Rekonstruktion der Augenoberfläche zu behandeln. Um dies zu erreichen, wird die Auswirkungen des Einbaus von verschiedenen Medikamenten (wie Dexamethason, NGF und Bevacizumab) in die beiden Matrizen in vitro und in vivo untersucht.

